本网讯 近日,我校动物医学院兽医传染病学课题组孙裴教授团队携手动物科技学院殷宗俊教授团队在国际权威学术期刊《Journal of Virology》发表了题为“3A and 2B proteins of SVA play chess game with host restriction factor DDX23 by apoptotic pathway”的研究论文。揭示了A型塞内卡病毒的3A和2B非结构蛋白如何通过凋亡途径与宿主DEAD-box RNA解旋酶23(DEAD-box helicase 23, DDX23)展开相互调控。该研究首次阐明了DDX23抑制SVA复制的机制,以及病毒的反制策略。这为理解病毒-宿主互动提供了新视角,并为针对性抗病毒策略和疫苗开发奠定基础。

塞内卡病毒A(Senecavirus A,SVA)作为小RNA病毒科成员之一,感染猪群后可导致水疱病样症状并显著影响新生仔猪存活率。当下,SVA感染成为全球猪业可持续发展的障碍,亟需阐明其致病机制。DEAD-box RNA解旋酶家族以保守的DEAD(Asp-Glu-Ala-Asp)基序为特征,参与RNA代谢,包括转录、剪接和翻译。其中DDX23作为U5小核糖核蛋白的核心组分,主要调控RNA剪接,并参与核苷酸代谢和肿瘤信号传导。前期研究表明,DDX23在水疱性口炎病毒(VSV)感染中激活先天免疫,但其在SVA感染中的功能尚未明确。
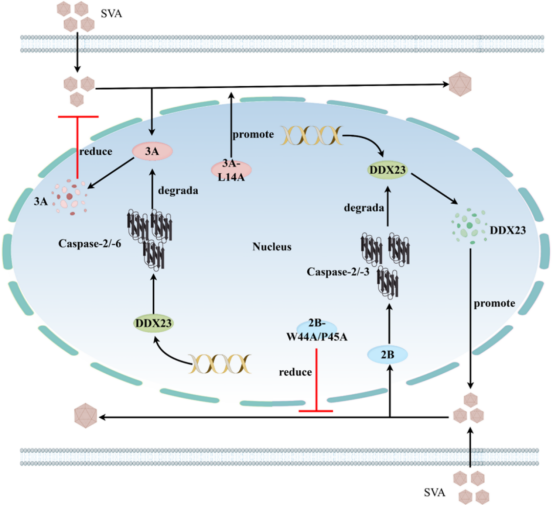
本研究从猪源DDX家族基因子集筛选入手,通过过表达、敲除、抑制剂处理和反向遗传学等方法,首次系统揭示DDX23通过Caspase-2/-6途径靶向SVA-3A的L14位点降解病毒蛋白以抑制复制,而SVA-2B通过Caspase-2/-3途径靶向DDX23-W44/P45位点以降解DDX23而对抗宿主防御,形成动态平衡。这一机制扩展了DEAD-box家族在小RNA病毒感染中的功能,强调Caspase途径在病毒-宿主互动中的双向调控作用。研究指出,这些发现为理解SVA的致病机制和免疫逃逸策略提供了重要基础,关键氨基酸L14、W44/P45可作为潜在的抗病毒靶点。该结果也将有助于缓解SVA对猪业的经济和健康压力,推动精准抗病毒策略的开发。
本研究工作共同通讯作者为我校孙裴教授、殷宗俊教授、李亮副教授和常馨月教授,博士研究生李杰、硕士研究生周易、林海成(已毕业)为共同第一作者,刘雪兰副教授及硕士研究生雷宗恒、毕瑞敏和王璇等对本研究做出了重要贡献。安徽农业大学为本研究的唯一通讯作者单位。本研究得到国家自然科学基金、安徽省自然科学基金、农业生物育种重大专项、安徽省农业产业技术体系(生猪)和安徽农业大学引进人才等项目资助支持。(文图:李亮 初审:王希春 复审:郑雪林 终审:曹雷)
论文链接:https://pubmed.ncbi.nlm.nih.gov/40956085/
